1 Was hat die EMA am Freitag entschieden?
Die EMA hat am Freitag das Vakzin von Biontech/Pfizerfür die Altersgruppe zwischen zwölf und 15 Jahren zugelassen. Bislang lag die Altersgrenze bei 16 Jahren. Über Zwölfjährigen wird dieselbe Dosis verabreicht wie auch allen älteren Gruppen.
2 Welche Daten liegen zum Vakzin von Biontech/Pfizer vor?
Biontech/Pfizer hat eine Studie mit Daten von insgesamt 2260 Kindern zwischen zwölf und 15 Jahren vorgelegt, diese wurde auch im Fachmagazin „New England Journal of Medicine“ publiziert. Die Kinder hatten im Abstand von 21 Tagen zwei Dosen des Impfstoffes (1131 Kinder) oder Placebo-Spritzen mit Kochsalzlösung (1129 Kinder) erhalten. In den USA wird Comirnaty schon seit 10. Mai an diese Altersgruppe verimpft, auch Kanada hat das Vakzin schon für Jugendliche freigegeben. Experte Markus Zeitlinger von der MedUni Wien gibt zu bedenken: „Die Gruppe der jungen Erwachsenen, die vom Alter an die Gruppe der Zwölf- bis 16-Jährigen angrenzt, ist jene Population, mit welcher wir die längste Erfahrung haben.“ Hier habe man Daten schon vor einem Jahr im Rahmen der Phase-I- und -II-Studien sammeln können. „In Bezug auf das Immunsystem ist etwa ein 15-Jähriger von einem 18-Jährigen nicht sehr weit entfernt.“
3 Welche Impfreaktionen sind bekannt?
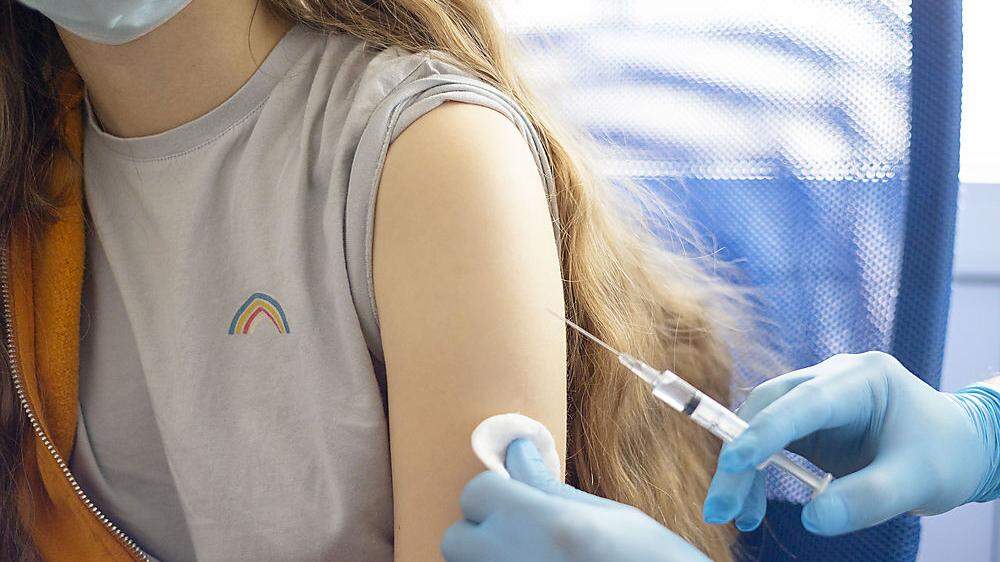
In der zuvor zitierten Studie wurden für jeweils sieben Tage nach den Injektionen Impfreaktionen dokumentiert. Unerwünschte Wirkungen wurden bis zu sechs Monate nach der zweiten Spritze erfasst. „Im Hinblick auf die Impfreaktionen ist es 1:1 das gleiche Bild wie auch bei den älteren Gruppen“, sagt Zeitlinger. Impfreaktionen waren mild bis moderat. Es handelte sich um Schmerzen an der Einstichstelle, Müdigkeit, Kopfschmerzen und Fieber – nach der zweiten Dosis häufiger als nach der ersten. Die Beschwerden verschwanden innerhalb von wenigen Tagen. Schwerere unerwünschte Wirkungen wie Thrombosen oder anaphylaktische Schocks traten nicht auf.
4 Wie wirksam ist der Impfstoff?
Die Wirksamkeit einer zweifachen Impfung lag den Forschern zufolge bei 100 Prozent, da es in der Studiengruppe im Vergleich zur Placebo-Gruppe keinen Covid-19-Fall gegeben habe. Abgesehen davon zeigten auch Labortests, dass die Impfung eine stabile Immunantwort erzeugte, sie war sogar besser als in der Gruppe der Jugendlichen und jungen Erwachsenen zwischen 16 und 25 Jahren.
5 Wie werden Vakzine für Kinder überprüft?
Bei Studien, die Sicherheit und Wirksamkeit bei Kindern als Untersuchungsgegenstand haben, handelt es sich um sogenannte Dosisfindungsstudien. Es geht darum, herauszufinden, welche Dosierung des Impfstoffes, der Erwachsenen verabreicht wird, in Kindern die beste Wirkung mit den geringsten unerwünschten Reaktionen hervorruft. Es werden unterschiedliche Dosierungen bzw. ihre Auswirkungen untersucht: So werden etwa Halb- oder Vierteldosen verabreicht. Sie umfassen weniger Probanden als etwa die großen Phase-III-Studien zur eigentlichen Zulassung eines Vakzins.
6 Wie werden Nutzen bzw. Risiko in Bezug auf die Kinderimpfungen von der EMA beurteilt?
Die EMA basiert die Zulassung auf der Nutzen-Risiko-Abwägung für das Individuum. „Der Impfstoff würde nicht zugelassen werden, wenn nicht für das individuelle Kind ein positiver Effekt vorliegen würde“, sagt Zeitlinger. Die EMA könne kein Medikament zulassen, um etwa den Herdenschutz zu erreichen.
7 Wieso müssen Kinder überhaupt geimpft werden?
Kinder und Jugendliche können, wenn auch seltener, ebenso an Covid-19 erkranken. Bei Kindern kann in sehr seltenen Fällen PIMS, eine überschießende Reaktion des Immunsystems, auftreten. Auch sind sie von Long Covid betroffen. „Gerade diese chronischen Leiden dürften bei Kindern etwas häufiger sein, als man sich bewusst ist“, sagt Zeitlinger.
8 Wann können in Österreich die ersten über Zwölfjährigen geimpft werden?
Der Plan des Gesundheitsministeriums ist, Zwölf- bis 15-Jährigen über den Sommer Impfangebote zu machen.